LudgerTag™ 2-AB(2-氨基苯甲酰胺)多糖标记试剂盒(货号:LT-KAB-A2)包含经胺化还原反应使染料结合在多糖未结合还原端基的试剂,使用2-氨基苯甲酰胺(2-AB)标记未结合多糖。
应用:用2-氨基苯甲酰胺(2-AB)标记未结合多糖
染料性质
分子量 136.15
荧光 λex(染料) = 320 nm, λem = 420 nm
结构
样品数:通常每套标记试剂最多可分析15个独立样品。
样品量:每个样品含25pmol到25nmol多糖。
适合检测的样品:任何带有未结合还原末端的纯化聚糖,都可以进行标记。
结构完整性:未发现唾液酸、标记效率:通常大于85%(取决于样品)。
标记选择性:本质上是化学计量标记。
储存:室温下暗处储存。远离热源、避光和防潮。所供试剂至少可稳定保存两年。
运输:该产品可在室温下运输。
处置:使用时涉及的任何玻璃或塑料器皿以及溶剂,应确保不含糖化酶及外源性碳水化合物。在所有样品处理时,使用无粉末手套,避免受到外源性碳水化合物的污染。标记试剂设计的所有步骤都必须在干燥环境下操作,并使用干燥的玻璃和塑料器皿。一旦打开试剂瓶,应立即使用。多余试剂根据当地安全规则丢弃。
安全:仅供研究用。不得用于人体或药用。请阅读安全数据表(SDS)了解所有相关化学品。标记试剂涉及的任何操作,都应配备使用适当的个人安全保护装置 – 眼镜、耐化学性手套(如 腈类手套),以及在实验室通风柜进行操作。
试剂盒组成
每个标记试剂盒包括1瓶以下试剂:
| Cat. |
# Item |
Quantity |
| LT-2AB-01 |
2-AB染料 (2-氨基苯甲酰胺) |
5 mg |
| LT-DMSO-01 |
二甲基亚砜 DMSO |
350 μl |
| LT-ACETIC-01 |
冰醋酸 |
500 μL |
| LT-CYANOB-01 |
氰基硼氢化钠(还原剂) |
6 mg |
所需的其他试剂和设备
- 加热模块、炉或相近功能的干热器(不能使用水浴),设定在65°C
- 旋转蒸发仪(例如Savant, Heto, 或其它)
- 反应小瓶 (e.g. 聚丙烯 微量离心瓶)
- 注:如果进行样品标记后洗涤(参见样品洗涤部分),则需要其它试剂。
标记操作时间线
LudgerTag 标记过程,加上可选样品标记后洗涤,通常需要4-5个小时:
| 过程 |
时间 |
总时间(小时) |
| 样品转移到反应瓶并干燥 |
30分钟 |
0.5 |
| 配置并加入标记试剂 |
15分钟 |
0.75 |
| 样品和试剂一起培养 |
3 小时 |
3.75 |
| 标记后洗涤 |
1小时 |
4.75 |
还原性胺化
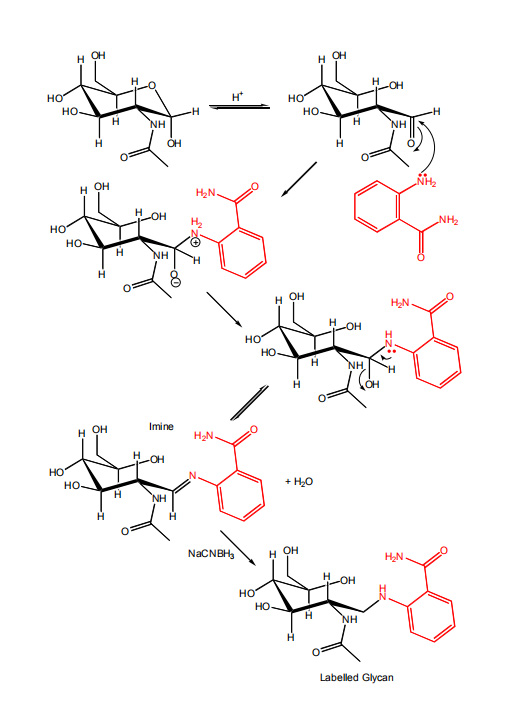
标记反应涉及一个两步反应过程。 (见图1):
1.希夫碱生成
具有未结合还原末端的多糖,其末端在闭环(有环)和开环(无环)状态之间处于平衡状态。染料的伯胺对无环还原端基残基的羰基碳进行亲核进攻,形成部分稳定的席夫碱。
2. 希夫碱还原
希夫碱亚胺基通过化学还原生成稳定标记的多糖。
图1:通过还原性胺化反应,用2-氨基苯甲酰胺标记多糖
标记操作概述
LudgerTag 多糖标记试剂盒,用于荧光或发色标记带有为结合还原端基的多糖。在所中色谱和结构序列分析中,经标记的多糖既可以进行高灵敏度荧光检测,也可以进行紫外吸收监测,包括使用LudgerSep液相色谱柱的色谱分析和使用外切糖苷酶的序列分析(参见 参考1-5, 7)。
标记过程概述如下:
1 多糖准备
准备多糖样品,去除类似盐和洗涤剂等可能干扰标记过程的污染物。
2 多糖干燥
将样品置于反应小瓶中干燥。
3 标记试剂准备
将试剂盒中相关试剂混合制备新鲜的染料标记溶液。
4 将标记试剂加入多糖中
将小量的标记溶液加入每一份多糖样品中
5 培养
培养样品使标记反应进行下去。
6 标记后洗涤
培养完成后,如有必要(根据后续分析过程而定),直接进入洗涤流程以去除过量的标记试剂。.
7 经标记的多糖储存或者分析
经标记的多糖样品现在可以用于分析了。
样品准备
要进行标记的多糖样品,无论是纯化的或是多糖混合物,必须包含未结合的还原端基,颗粒状且不含无机盐,并溶于易挥发的溶剂体系中(最好是纯水)。
下列物质可能干扰标记反应,必须在进行LudgerTag™ 标记之前,事先从多糖样品中去除:
不挥发溶剂
不挥发盐,尤其是过渡金属离子
洗涤剂
染料和染色剂,例如考马斯蓝
Ludger提供了一系列LudgerClean™试剂盒,用于在Ludgertag™标记之前洗涤多糖样品。这些内容在LudgerClean多糖洗涤指南[参考6]中有详细说明。
标准样品制备概述如下:
1 多糖纯化
如有必要,从样品中按照多糖洗涤指南[参考6]中所述去除非碳水化合物污染物。
2 将样品转移至反应小瓶中
从典型糖蛋白中获得的多糖,样品量应在100个皮摩尔-50纳米摩尔的范围内。单一的纯多糖,即使仅有5皮摩尔的量,也可以被标记,并在之后高效液相色谱分析中检测出。适用的反应小瓶,包括小型聚丙烯微离心管和可用于PCR操作的试管。
3 样品干燥
理论上,应使用旋转蒸发器干燥样品。如果条件不允许,可以小心使用冷冻干燥(尤其要确保在小瓶的最底部的样品,冻干成小而致密的物质)。 不要将样品置于高温(>28℃)或极端pH环境下,因为这样会导致唾液酸在酸催化下耗损(高温、强酸),或多糖还原端的异构反应(强碱)。
标记试剂准备
按如下过程制备新鲜标记试剂:
4 制备DMSO-醋酸混合液
150μl冰醋酸加入盛有DMSO的小瓶中,并用移液器抽吸混合。
冰醋酸和DMSO的货号分别为LT-ACETIC-01和 LT-DMSO-01。
小心敲击安瓿瓶以震落附着安瓿上半部的内容物,然后小心打开安瓿瓶。
如果DMSO冻成固体,在烘箱或加热快上在30-65℃之间缓慢加热小瓶(在启封前)。
5 加入染料
将100μl DMSO-醋酸混合液加入LudgerTag™ 2-AB (2-氨基苯甲酰胺) 染料小瓶中,混合直至染料完全溶解。
染料货号为LT-2AB-01。
6 加入还原剂
将溶解的染料加入盛有LudgerTag™ 氰基硼氢化钠 (还原剂) 的小瓶中,使用移液器抽吸混合直至还原剂完全溶解形成最终的标记试剂。
氰基硼氢化钠还原剂的货号是LT-CYANOB-01。
如果还原剂难以溶解,那么在65℃的恒温培养箱中,或者加热块上,轻缓地加热至多4分钟。如还原剂仍未全溶,补加10μl纯水并混合均匀。
标记试剂应防潮,并在配置60分钟内使用。
标记反应
7 将标记试剂加入样品
将5μl标记试剂加入到每一份经干燥的多糖样品中,盖上离心管,彻底混合,然后轻轻敲击以确保标记溶液位于小瓶的底部。
8 培养
将反应小瓶放在65℃的加热块、砂浴或烘箱中,培养3小时。
培养必须在干燥的环境下进行。请使用培养箱或干燥块,请务必不要使用水浴。
样品必须完全溶解在标记溶液中,才能有效进行标记。为了促进完全溶解,样品可在培养温度达到65℃后涡旋混合30分钟,然后继续培养。
在大多数情况下,培养时间可以缩短至2小时或延长至4小时,而不会显著改变标记反应结果。
9 离心并冷却
培养结束后取出样品,短暂离心微量试管,并让其完全冷却至室温。
LudgerClean™ S 标记后样品洗涤
对于特定的应用 – 例如后续的HPLC分析,标记后的样品洗涤(去除多余的染料和其它标记试剂) 是必不可少的。使用LudgerClean™ S 小柱 (货号 LC-S-Ax, 此处x代表试剂盒中小柱的数量)按试剂盒所附标准操作程序可以完成样品洗涤。
对于过量标记试剂不会影响后续样品分析的应用而言,样品标记后洗涤并非必需。这些分析手段包括碳水化合物电泳,游离染料会从标记多糖条带处分离开。
LudgerTag™ 2AA标记多糖的分析
LudgerTag™ 2-AB标记多糖可通过一系列分析方法进行研究,包括HPLC,凝胶电泳和质谱。 这些会在参考资料8里详细叙述,在下文也有概述。
高压液相色谱分析
LudgerTag™ 2-AB标记多糖混合物可以通过一系列HPLC(高压液相色谱)方法进行分离和分析,也包括LudgerSep HPLC:
|
分析类型
|
柱子
|
货号
|
|
带电荷和中性多糖的分离
|
LudgerSep™ C
|
LS-C-01
|
|
带电荷和中性多糖的剖面分析
|
LudgerSep™ N
|
LS-N-01
|
|
中性多糖的分离
|
LudgerSep™ R
|
LS-R-01
|
上述多糖分析柱的使用在参考4和参考8里有概述。
对于从复杂多糖混合物中纯化和分析LudgerTag?标记寡糖而言,LudgerSep? N柱是非常有效的分析工具。
关于您的特殊应用,请联系我们获取建议。
酶法分析
高纯度,测序级酶(例如外切糖苷酶),适合N-和O-链接LudgerTag™ 标记多糖的结构分析,许多公司有市售产品。
选择糖苷酶时,尤其应注意选择配方与您专属应用匹配的产品。例如,部分酶和缓冲液拥有会干扰特定分析手段的组份。在选则您工作所需的酶和反应条件时,请致电我们获取指导。
质谱和电泳
LudgerTag™ 标记多糖也可以用质谱、电泳和其它光谱分析手段进行分析。如果您想确定最合适的分析条件,请来电咨询。
参考文献及相关文献
1 Bigge, J.C.; Patel, T.P; Bruce, J.A.; Goulding, P.N.; Charles, S.M; Parekh, R.B. (1995) ‘Non-selective and efficient fluorescent labeling of glycans using 2-aminobenzamide and anthranilic acid‘. Analytical Biochemistry 230: 229-238
2 Guile, G.R.; Rudd, P.M.; Wing, D.R.; Prime, S.B.; Dwek, R.A. (1996) ‘A rapid and high-resolution high-performance liquid chromatographic method for separating glycan mixtures and analyzing oligosaccharide profiles‘. Analytical Biochemistry 240: 210-226
3 Townsend, R.R.; Lipniunas, P.H.; Bigge, C.; Ventom, A.; Parekh, R. (1996) ‘Multimode high-performance liquid chromatography of fluorescently labeled oligosaccharides from glycoproteins‘.Analytical Biochemistry 239: 200-207
4 LudgerSep High Resolution HPLC Carbohydrate Profiling Guide (Cat # LS-GUIDE-01)
5 Ludger Enzyme Selection Guide (Cat # EZ-GUIDE-01)
6 LudgerClean Glycan Cleanup Guide (Cat # LC-GUIDE-01)
7 Hardy, M.R. (1997)‘Glycan labeling with the fluorophores 2-aminobenzamide and anthranilic acid’in ‘Techniques in Glycobiology’, edited by Townsend, R.R and Hotchkiss, A.T.. Marcel Dekker Inc, New York .
8 Ludger Technical Note # TN-AB-01: Analysis of 2-AB (2-aminobenzamide) labeled glycans
故障排除
Ludgertag?标记过程是一种高效、可靠的方法。如果出现问题,通常可以毫无毫不费力地予以纠正。以下是最有可能出现的问题、可能的原因和解决方案。
染料结合率低 / 标记收率低
标记温度不正确
请确保烘箱或加热块预设与培养温度相称,并确保反应管在标记时始终处于该温度下。
样品未完全溶解
多糖必须完全溶解在标记混合溶液中,标记效率才能最大化。
请确保在培养操作之前,样品与标记试剂完全混合均匀。作为预防措施,在培养开始后,继续仔细搅拌样品15分钟。
样品中含有干扰标记的污染物。
在标记之前,请确认多糖得到充分纯化(参见操作步骤1和 LudgerClean? 多糖洗涤指南)
标记溶液无效。
请务必在使用前即刻配置标记溶液 – 试剂在混合后的几小时内即会失活。
启动时多糖较原先预估的要少
多糖不含未结合的还原基团。
2-AB染料通过未结合的还原端的醛基与多糖结合。糖醇和还原端基已经结合的多糖 (例如糖肽,糖脂和已标记多糖)不含未结合还原端基,因此无法和染料结合。
在标记后洗涤时多糖损耗。
请确认已经按照洗涤规程去除多余标记试剂,且洗涤试剂正确配制。
标记样品中含有带荧光的非碳水化合物
原始的多糖中含有醛稳定污染物。
请确认多糖在标记前已经充分纯化(参见操作步骤1和LudgerClean多糖洗涤指南)。
标记后洗涤步骤未正常工作
请确认已经按照洗涤规程去除多余标记试剂,且洗涤试剂正确配制。
较小分子量多糖选择性损耗
洗涤小柱未正确填充
请确保小柱已经正确充填,样品上盘时,柱床已经用乙腈浸润。
标记后洗涤时是否使用了不当清洗剂。
请确保清洗剂正确配制。
较大分子量多糖选择性损耗
样品未完全溶解
多糖必须完全溶解于标记混合物中以获得最大标记效率。 较大的多糖较小分子糖更难溶于标记混合物中。请确保样品在培养前与标记试剂充分混合,可以在培养开始后再小心混合样品15分钟,以作为预防措施。
多糖去唾液酸化
样品在高温下水溶液中呈酸性。
避免唾液酸化多糖样品溶液长时间处于酸性和高温环境下。注意还原胺化反应是在无水条件下进行的,在此条件下唾液酸的损失最小。
通常,样品保存在5-8.5的溶液中,避免暴露在30℃以上的温度下。样品溶于pH缓冲溶液(pH介于5和8.5之间),即使在高于30℃的温度下,也往往能够抵抗酸催化的去唾液酸反应。即使这样,也要谨慎行事,尽可能保持样品冷却。
样品标记后没有正确洗涤
确保样品在还原胺化反应后立即进行标记后洗涤,且标记后的干燥和洗涤应金肯能快地进行。
未经干燥和随后洗涤的标记样品容易发生酸催化去唾液酸反应。